👉Enunciado: Una solución de 6.85 g de un carbohidrato en 100.0 g de agua tiene una densidad de 1.024 g / mL y una presión osmótica de 4.61 atm a 20.0 ° C. Calcula la masa molar del carbohidrato.
Mas
ejercicios resueltos de química sobre #propiedadesdelasdisoluciones. Mas
ejercicios resueltos de otros capítulos de #química. Curso
de #propiedadesdelasdisoluciones. ¡Si
te gustó, suscríbete!
👉Demostración de las ecuaciones clave:
https://quimicadejoselegcuantitativa.blogspot.com/2021/08/coligativas-osmosis.html
https://quimicadejoseleg-lamateria.blogspot.com/2021/06/analisis-de-composicion.html
👉Solución:
Usaremos la masa molar a partir de la presión osmótica, ecuación que dedujimos en el ejercicio 12.64. Pero en este caso el volumen de la solución si puede ser calculado con precisión ya que tenesmos las masas de los dos compuestos mezclados y la densidad total. Reemplazamos el volumen de la solución como el cociente de masa y densidad, y dicha masa como la suma de masas de soluto y solvente. Finalmente expresamos de manera elegante.
Reemplazamos
👉Otros enunciados: Cual es la masa molar
de 6.85 g de carbohidrato en 100 g H2O a presión osmótica 4.61 atm, Determine la
masa molar de 6.85 g de carbohidrato en 100 g H2O a presión osmótica 4.61 atm, Determinar
la masa molar de 6.85 g de carbohidrato en 100 g H2O a presión osmótica 4.61
atm, Calcule la masa molar de 6.85 g de carbohidrato en 100 g H2O a presión
osmótica 4.61 atm, Calcular la masa molar de 6.85 g de carbohidrato en 100 g H2O
a presión osmótica 4.61 atm, Halle la masa molar de 6.85 g de carbohidrato en
100 g H2O a presión osmótica 4.61 atm, Hallar la masa molar de 6.85 g de carbohidrato
en 100 g H2O a presión osmótica 4.61 atm,
👉Temas:
química, química general, disoluciones, propiedades de las disoluciones,
solubilidad, presión osmótica,


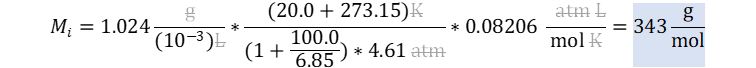

No hay comentarios:
Publicar un comentario