👉Enunciado: Se disuelve una cantidad de 7.480 g de un compuesto orgánico en agua para obtener 300.0 mL de solución. La solución tiene una presión osmótica de 1.43 atm a 27 °C. El análisis de este compuesto muestra que contiene 41.8 por ciento de C, 4.7 por ciento de H, 37.3 por ciento de O y 16.3 por ciento de N. Calcule la fórmula molecular del compuesto.
Mas
ejercicios resueltos de química sobre #propiedadesdelasdisoluciones. Mas
ejercicios resueltos de otros capítulos de #química. Curso
de #propiedadesdelasdisoluciones. ¡Si
te gustó, suscríbete!
👉Demostración de las ecuaciones clave:
https://quimicadejoselegcuantitativa.blogspot.com/2021/08/coligativas-osmosis.html
https://quimicadejoseleg-lamateria.blogspot.com/2021/06/analisis-de-composicion.html
👉Solución:
Usaremos la masa molar a partir de la presión osmótica,
ecuación que dedujimos en el
ejercicio 12.64.
Con esa masa molar podemos aplicar la función para calcular subíndices
de una fórmula molecular dada en la sección de análisis
de composición.
Asumiendo para este segundo cálculo que tenemos una segunda muestra de 100 g y por ende la masa total es 100 g y la de cada elemento igual a su valor porcentual, pero en gramos. Ahora operamos:
En este caso la masa de soluto es 100 g porque asumimos una muestra diferente en un experimento diferente.
Por lo tanto, la fórmula molecular es C15H20O10N5.
👉Otros enunciados: Cual es la fórmula
molecular de 41.8% C 4.7%H 37.3% O 16.3%N a presión osmótica 1.43 atm, Determine
la fórmula molecular de 41.8% C 4.7%H 37.3% O 16.3%N a presión osmótica 1.43
atm, Determinar la fórmula molecular de 41.8% C 4.7%H 37.3% O 16.3%N a presión
osmótica 1.43 atm, Calcule la fórmula molecular de 41.8% C 4.7%H 37.3% O 16.3%N
a presión osmótica 1.43 atm, Calcular la fórmula molecular de 41.8% C 4.7%H
37.3% O 16.3%N a presión osmótica 1.43 atm, Halle la fórmula molecular de 41.8%
C 4.7%H 37.3% O 16.3%N a presión osmótica 1.43 atm, Hallar la fórmula molecular
de 41.8% C 4.7%H 37.3% O 16.3%N a presión osmótica 1.43 atm,
👉Temas:
química, química general, disoluciones, propiedades de las disoluciones,
solubilidad, presión osmótica, análisis de composición porcentual




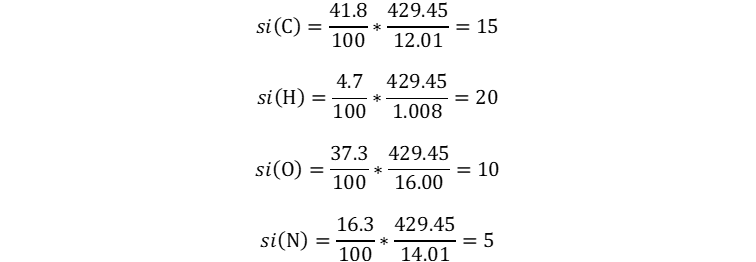

No hay comentarios:
Publicar un comentario