(Ciencias de Joseleg)
(Química) (Química cuantitativa) (Termoquímica)
(Ejercicios) (Introducción)
(Historia)
(Energía)
(Sistema,
alrededores y calor) (Primera
ley de la termodinámica) (Entalpía)
(Entalpía
de la reacción) (Capacidad
calorífica y calor específico) (Calorimetría
a volumen constante) (Calorimetría
a presión constante) (Ley
de Hess) (Entalpía
de formación) (Calor
de solución y disolución) (Termoquímica
de los alimentos) (Termoquímica
de los combustibles) (Energía
del futuro) (Referencias
bibliográficas)
La mayoría de las reacciones químicas utilizadas para la producción de
calor son reacciones de combustión. La energía liberada cuando se quema un
gramo de cualquier sustancia es el valor
combustible de la sustancia. El valor de combustible de cualquier
alimento o combustible se puede medir por calorimetría.
La
glucosa como fuente de energía
La mayor parte de la energía que nuestro cuerpo necesita proviene de los
carbohidratos y las grasas. Los carbohidratos conocidos como almidones se
descomponen en los intestinos en glucosa, C6H12O6.
La glucosa es soluble en sangre y en el cuerpo humano se la conoce como azúcar
en sangre. Es transportada por la sangre a las células donde reacciona con el O2
en una serie de pasos que puede estudiar en los capítulos de glucólisis y respiración celular, produciendo
finalmente CO2(g), H2O(l) y energía con una entalpía
estándar de -2803 kJ/mol de reacción (o de glucosa, es este caso da lo mismo).
Debido a que los carbohidratos se descomponen rápidamente, su energía se
suministra rápidamente al cuerpo. Sin embargo, el cuerpo almacena solo una
cantidad muy pequeña de carbohidratos. El valor medio de combustible de los
carbohidratos es 17 kJ/g o 4 kcal/g.
Las
grasas como fuente de energía
Al igual que los carbohidratos, las grasas producen CO2 y H2O
cuando se metabolizan. La reacción de la triestearina, C57H110O6,
una grasa típica genera una entalpía estándar de 275520 kJ/mol de reacción.
El cuerpo utiliza la energía química de los alimentos para mantener la
temperatura corporal, contraer los músculos y construir y reparar tejidos.
Cualquier exceso de energía se almacena en forma de grasas. Las grasas son
adecuadas para servir como reserva de energía del cuerpo por al menos dos
razones:
👉 son insolubles en agua, lo que facilita el almacenamiento en el cuerpo, y …
👉 producen más energía por gramo que las proteínas o los carbohidratos, …
… que las convierte en fuentes de energía compactas. El valor medio de las
grasas en el combustible es 38 kJ/g o 9 kcal/g.
Midiendo
la entalpía de una reacción en un paso o en múltiples pasos
La combustión de carbohidratos y grasas en un calorímetro de bomba genera
los mismos productos que cuando se metabolizan en el cuerpo. Aunque evidentemente
en el cuerpo las sustancias orgánicas no se oxidan en una combustión, o si no
arderíamos espontáneamente, lo que sucede es que la entalpía estándar de una
reacción ∆H0 al ser una variable de estado,
tiene el mismo valor sin importar que se haga en un solo paso
de combustión en un calorímetro de bomba o que se haga en un sinfín de pequeños pasos como ocurre en un
proceso metabólico biológico.
Proteínas
como fuentes de energía
El metabolismo de las proteínas produce menos energía que la combustión en
un calorímetro porque los productos son diferentes. Las proteínas contienen
nitrógeno, que se libera en el calorímetro de bomba como N2. En el
cuerpo, este nitrógeno termina principalmente como urea, (NH2)2CO.
El cuerpo utiliza las proteínas principalmente como materiales de construcción
para las paredes de los órganos, la piel, el cabello, los músculos, etc. En
promedio, el metabolismo de las proteínas produce 17 kJ/g o 14 kcal/g, lo mismo
que para los carbohidratos.
Tablas
de valor de combustible en alimentos
Los
valores de combustible para algunos alimentos comunes se muestran en la siguente
tabla:
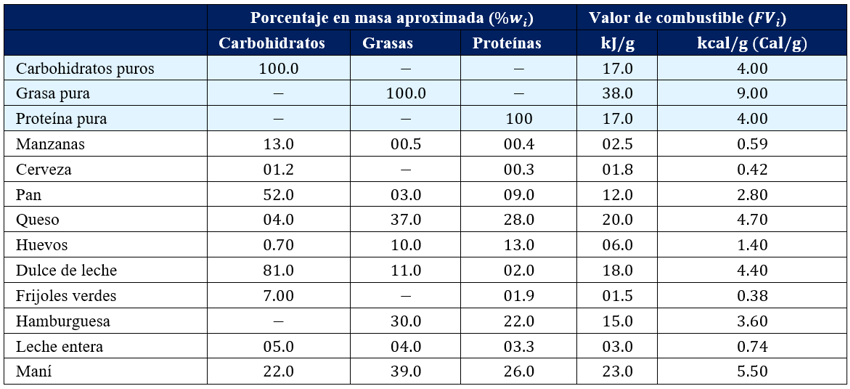
Tabla 14‑1. Composiciones y valores de combustible de algunos alimentos comunes.Tomada de la Química La Ciencia
Central (Brown et al., 2017). Tenga en cuenta que los alimentos presentados
aquí se toman como mezclas de sustancias con sus propios valores de combustible
promedio. Algunos alimentos tienen proporciones muy bajas de algunos nutrientes,
por ejemplo la mantequilla contendrá muy pocos carbohidratos o proteínas en
comparación con la proporción en grasa que posee, por tal razón en la tabla
cuando eso sucede se coloca un guion.
Las
etiquetas de los alimentos envasados muestran las cantidades de carbohidratos,
grasas y proteínas contenidas en una porción promedio, así como la cantidad de
energía suministrada por una porción. La cantidad de energía que nuestro cuerpo
necesita varía considerablemente, dependiendo de factores como el peso, la edad
y la actividad muscular. Se requieren aproximadamente 100 kJ por kilogramo de
masa corporal por día para mantener el funcionamiento del cuerpo a un nivel
mínimo. Una persona promedio de 70 kg (154 libras) gasta alrededor de 800 kJ/h cuando
realiza un trabajo ligero, y la actividad intensa a menudo requiere 2000 kJ/h o
más. Cuando el valor de combustible, o el contenido calórico, de los alimentos
que ingerimos excede la energía que gastamos, nuestro cuerpo almacena el
excedente en forma de grasa.
Calculando
el valor de combustible
De
una sustancia pura
El valor de
la combustión va a ser igual al cociente que ocurre entre la entalpía estándar
de la reacción sobre la masa del compuesto clave.
De
una mezcla
Como vimos
anteriormente, los alimentos y algunos tipos de combustibles son en realidad
mezclas de sustancias y por lo tanto, se hace necesario pode calcular el valor
de combustible total.
De
una porción
El valor de
combustible de una porción va a tener unidades de energía únicamente ya que
ésta está dada para una masa arbitraria de la sustancia. Dado lo anterior
denominaremos a esta variable como Portion Fuel Value (PFV).
Variables de consumo y
porciones
La energía
de los alimentos se consume esencialmente por dos variables, el tiempo t o la
distancia recorrida x. ¿Cuántas porciones deben
consumirse para proporcionar la energía necesaria para mantener un determinado
rendimiento en un tiempo t o una distancia x?
Unidades de energía
Aunque ya
lo vimos en secciones anteriores, es relevante recordar que:
Una unidad de energía relacionada utilizada en nutrición es la Caloría
nutricional (tenga en cuenta la C mayúscula).
👉Enunciado:
Una porción de 28 g de un cereal de desayuno
popular servido con 120 ml de leche descremada proporciona 8 g de proteína (17
kJ/g), 26 g de carbohidratos (17 kJ/g) y 2 g de grasa (38 kJ/g). Utilizando los
valores de combustible promedio de estas sustancias, estime el valor de
combustible (contenido calórico) de esta porción // Pulse aquí.







No hay comentarios:
Publicar un comentario