👉Enunciado: ¿Cuál es la presión osmótica (en atm) de una solución acuosa 1.36 M de urea [(NH2)2CO] a 22.0 °C?
Mas
ejercicios resueltos de química sobre #propiedadesdelasdisoluciones. Mas
ejercicios resueltos de otros capítulos de #química. Curso
de #propiedadesdelasdisoluciones. ¡Si
te gustó, suscríbete!
👉Demostración de las ecuaciones clave:
https://quimicadejoselegcuantitativa.blogspot.com/2021/08/coligativas-osmosis.html
👉Solución: lo primero que debemos tener en cuenta es que la urea no es electrolítica y por lo tanto vamos a asumir a priori que su factor de van 't Hoff es igual a uno. Con lo anterior en mente empleamos la ley de presión osmótica, pero cancelando analíticamente el factor de van 't Hoff.
Reemplazamos teniendo en cuenta que molar no sirve para análisis
dimensional y por lo tanto lo reemplazamos por sus fundamentales mol/L.
👉Otros enunciados: Cual es la presión osmótica
de una solución de urea al 1.36 M y 22.0 °C, Determine la presión osmótica de
una solución de urea al 1.36 M y 22.0 °C, Determinar la presión osmótica de una
solución de urea al 1.36 M y 22.0 °C, Calcule la presión osmótica de una
solución de urea al 1.36 M y 22.0 °C, Calcular la presión osmótica de una
solución de urea al 1.36 M y 22.0 °C, Halle la presión osmótica de una solución
de urea al 1.36 M y 22.0 °C, Hallar la presión osmótica de una solución de urea
al 1.36 M y 22.0 °C,
👉Temas:
química, química general, disoluciones, propiedades de las disoluciones,
solubilidad, presión osmótica


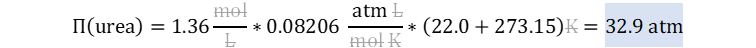

No hay comentarios:
Publicar un comentario