Enunciado Calcule los gramos contenidos en 1.00 ml de una solución al 0.100 N de SO3. (Nota, asuma que el azufre se reduce desde +6 hasta +4). Enlace a YouTube
Mas ejercicios resueltos de
química sobre #unidadesdeconcentracion. Mas ejercicios resueltos de
otros capítulos de #química. Curso de
#unidadesdeconcentración. ¡Si te gustó, suscríbete!
Demostración
de las ecuaciones clave:
https://quimicadejoselegcuantitativa.blogspot.com/2021/08/unidades-concentracion-conversiones.html
Solución:
Usaremos la
solución analítica que obtuvimos
para el ejercicio 10.9a.
Planteamos
una ecuación de reacción redox.
Calculamos el
equivalente molar usando como ion de referencia al electrón.
Calculamos la masa molar.
Reemplazamos
asumiendo que mili es igual a 10-3; y que normal es igual a eq/L.
Otros
enunciados: gramos en 1 ml de SO3 al 0.1 normal, masa en 1
ml de SO3 al 0.1 N, peso en 1 ml de SO3 al 0.1 eq/L, con 1ml de una solución 0.1
normal de SO3 hallar los gramos de soluto, con 1ml de una solución 0.1 N de SO3
calcular la masa de soluto, con 1ml de una solución 0.1 eq/l de SO3 hallar el
peso de soluto, hallar la masa en gramos de soluto con la concentración normal
y el volumen total de la solución
Temas: química, química general, unidades de
concentración, conversiones entre unidades de concentración, peso equivalente,
equivalente molar, factor equivalente, concentración normal, normalidad química





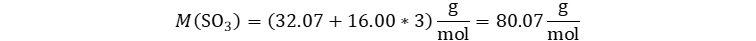


No hay comentarios:
Publicar un comentario