👉Enunciado: Si tiene 505 mL de solución HCl al 0.125 molar, y desea diluirla a 0.1 molar, ¿Cuánta agua debe agregar? Asuma de los volúmenes son aditivos.
Mas
ejercicios resueltos de química sobre #unidadesdeconcentracion. Mas
ejercicios resueltos de otros capítulos de #química. Curso
de #unidadesdeconcentración. ¡Si
te gustó, suscríbete!
👉Demostración de las ecuaciones clave:
https://quimicadejoselegcuantitativa.blogspot.com/2021/08/cambios-concentracion.html
👉Solución: Iniciamos asumiendo que la
cantidad de sustancia del HCl no cambia, en consecuencia podemos reemplazar las
cantidades inicial y final por lo que vale en términos de la concentración
molar. Como asumimos que los volúmenes son aditivos, entonces el volumen final
es igual a la suma del volumen inicial mas el volumen del solvente agregado.
Finalmente despejamos el volumen del solvente y expresamos la ecuación de
manera elegante.
Reemplazamos.
👉Otros enunciados: Cual es el volumen de
agua para diluir 505 mL HCl al 0.125 M hasta 0.1 M, Determine el volumen de
agua para diluir 505 mL HCl al 0.125 M hasta 0.1 M, Determinar el volumen de
agua para diluir 505 mL HCl al 0.125 M hasta 0.1 M, Obtenga el volumen de agua para
diluir 505 mL HCl al 0.125 M hasta 0.1 M, Obtener el volumen de agua para
diluir 505 mL HCl al 0.125 M hasta 0.1 M, Calcule el volumen de agua para
diluir 505 mL HCl al 0.125 M hasta 0.1 M, Calcular el volumen de agua para
diluir 505 mL HCl al 0.125 M hasta 0.1 M, Halle el volumen de agua para diluir
505 mL HCl al 0.125 M hasta 0.1 M, Hallar el volumen de agua para diluir 505 mL
HCl al 0.125 M hasta 0.1 M,
👉Temas: química,
química general, disoluciones, unidades de concentración, molaridad, concentración
molar, mol/L, preparar una solución de concentración molar, disolviendo una
solución, alícuota, C1V1=C2V2


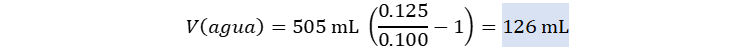

No hay comentarios:
Publicar un comentario