👉Enunciado: La densidad de una solución acuosa que contiene 10.0 por ciento de etanol (C2H5OH) en masa es 0.984 g / mL. ¿Qué volumen de la solución contendría 0.125 moles de etanol?
Mas
ejercicios resueltos de química sobre #unidadesdeconcentracion. Mas
ejercicios resueltos de otros capítulos de #química. Curso
de #unidadesdeconcentración. ¡Si te
gustó, suscríbete!
👉Demostración
de las ecuaciones clave:
https://quimicadejoselegcuantitativa.blogspot.com/2021/08/unidades-concentracion-conversiones.html
👉Solución: Usaremos la conversión
de fracción de masas a molaridad, reemplazamos molaridad por su definición y
despejamos el volumen total.
La fracción
de masas es igual a dividir el porcentaje en masa entre 100% por lo tanto su
valor para este caso es de wi = 0.100. Calculamos la masa
molar del soluto.
Reemplazamos mili por 10-3.
👉Otros
enunciados: Cual es el volumen de 0.125 moles de etanol al 10% y densidad 0.984 g/mL, Calcule el
volumen de 0.125 moles de etanol al 10% y densidad 0.984
g/mL, Determinar el volumen de 0.125 moles de etanol
al 10% y densidad 0.984 g/mL, Determine el volumen de 0.125
moles de etanol al 10% y densidad 0.984
g/mL, Obtenga el volumen de 0.125 moles de etanol
al 10% y densidad 0.984 g/mL, Calcule el volumen de 0.125
moles de etanol al 10% y densidad 0.984
g/mL, Obtener el volumen de 0.125 moles de etanol
al 10% y densidad 0.984 g/mL, Calcule el volumen de 0.125
moles de etanol al 10% y densidad 0.984
g/mL, Calcular el volumen de 0.125 moles de etanol
al 10% y densidad 0.984 g/mL, Halle el volumen de 0.125
moles de etanol al 10% y densidad 0.984
g/mL, Hallar el volumen de 0.125 moles de etanol
al 10% y densidad 0.984 g/mL,
👉Temas: química, química general, disoluciones, unidades de concentración, molaridad,
concentración molar, mol/L



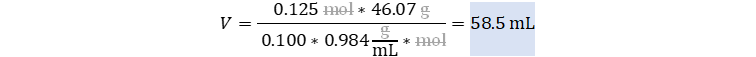

No hay comentarios:
Publicar un comentario