Descripción: Estequiometría gramo a gramo
Mas
ejercicios resueltos de química sobre estequiometría:
https://quimicadejoselegcuantitativa.blogspot.com/2021/08/ejercicios-problemas-estequiometria-resueltos.html
Mas ejercicios
resueltos de otros capítulos de química:
https://cienciasdejoseleg.blogspot.com/2021/09/problemas-de-quimica-resueltos.html
Para ver directo en YouTube:
Solución:
Usaremos
la solución analítica demostrada en el ejemplo 3.13
Calculamos
las masas molares de las dos sustancias involucradas, siendo sus valores 32.00
g/mol de O2 y 46.01 g/mol de NO2. Reemplazamos y calculamos:


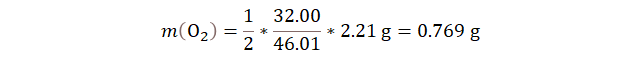

No hay comentarios:
Publicar un comentario