👉Enunciado: El análisis elemental de un sólido orgánico extraído de goma arábiga (una sustancia gomosa utilizada en adhesivos, tintas y productos farmacéuticos) mostró que contenía 40.0 por ciento de C, 6.7 por ciento de H y 53.3 por ciento de O. Una solución de 0.650 g del sólido en 27.8 g del disolvente difenilo dieron una depresión del punto de congelación de 1.56 °C. Calcule la masa molar y la fórmula molecular del sólido. (Kf para difenilo es 8.00 °C/m.)
Mas
ejercicios resueltos de química sobre #propiedadesdelasdisoluciones. Mas
ejercicios resueltos de otros capítulos de #química. Curso
de #propiedadesdelasdisoluciones. ¡Si
te gustó, suscríbete!
👉Demostración de las ecuaciones clave:
https://quimicadejoselegcuantitativa.blogspot.com/2021/08/coligativas-abulloscopico-crioscopico.html
https://quimicadejoseleg-lamateria.blogspot.com/2021/06/analisis-de-composicion.html
👉Solución: Como ese es un problema de análisis de composición porcentual, debemos buscar la ecuación clave para calcular subíndices dada en este enlace, y la modificamos para usar el porcentaje en peso.
Sin embargo, para poder conocer los subíndices, necesitamos la masa molar verdadera de la sustancia, usaremos la ley de descenso crioscópico, asumiendo a priori que la sustancia analizada es molecular y por ende no disociable, por lo que asumimos que su factor de van't Hoff vale 1 y lo cancelamos analíticamente.
Por lo tanto, ya contamos con dos soluciones analíticas, calcularemos
primero la masa molar verdadera, y luego los subíndices de cada elemento.
Ahora si podemos calcular los subíndices.
Por lo tanto, la fórmula molecular del difenilo es es C4H8O4.
👉Otros enunciados: Cual es la fórmula
molecular de 40.0% C 6.7% H y 53.3% O y descenso crioscópico de 1.56°C, Determine
la fórmula molecular de 40.0% C 6.7% H y 53.3% O y descenso crioscópico de 1.56°C,
Determinar la fórmula molecular de 40.0% C 6.7% H y 53.3% O y descenso crioscópico
de 1.56°C, Calcule la fórmula molecular de 40.0% C 6.7% H y 53.3% O y descenso crioscópico
de 1.56°C, Calcular la fórmula molecular de 40.0% C 6.7% H y 53.3% O y descenso
crioscópico de 1.56°C, Halle la fórmula molecular de 40.0% C 6.7% H y 53.3% O y
descenso crioscópico de 1.56°C, Hallar la fórmula molecular de 40.0% C 6.7% H y
53.3% O y descenso crioscópico de 1.56°C,
👉Temas:
química, química general, disoluciones, propiedades de las disoluciones,
solubilidad, aumento ebulloscópico, descenso crioscópico,




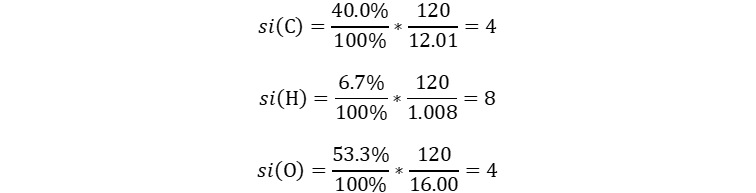

No hay comentarios:
Publicar un comentario