👉Enunciado: Calcular la molalidad de una solución acuosa al 35.4 por ciento (en masa) de ácido fosfórico (H3PO4). La masa molar del ácido fosfórico es de 97.99 g.
Mas
ejercicios resueltos de química sobre #unidadesdeconcentracion. Mas
ejercicios resueltos de otros capítulos de #química. Curso
de #unidadesdeconcentración. ¡Si
te gustó, suscríbete!
👉Demostración de las ecuaciones clave:
https://quimicadejoselegcuantitativa.blogspot.com/2021/08/unidades-concentracion-molalidad.html
https://quimicadejoselegcuantitativa.blogspot.com/2021/08/unidades-concentracion-conversiones.html
👉Solución: Aplicamos la solución analítica
planteada en este enlace.
Dado que la solución está
planteada para la fracción de masas, dividimos el porcentaje del enunciado
entre 100% con lo que obtenemos un valor de 0.354. Reemplazamos teniendo en
cuenta que un gramo es la milésima parte de un kilogramo o 10-3 kg.
Usamos la masa molar en sus unidades modernas, es decir 97.99 g/mol.
👉Otros enunciados: Cual es la molalidad
de H3PO4 al 35.4% en peso, Determine la molalidad de H3PO4 al 35.4% en peso, Determinar la molalidad de H3PO4 al 35.4% en peso, Obtenga la molalidad de H3PO4 al 35.4% en peso, Obtener la molalidad de H3PO4 al 35.4% en peso, Calcule la molalidad de H3PO4 al 35.4% en peso, Calcular la molalidad de H3PO4 al 35.4% en peso, Halle la molalidad de H3PO4 al 35.4% en peso, Hallar la molalidad de H3PO4 al 35.4% en peso,


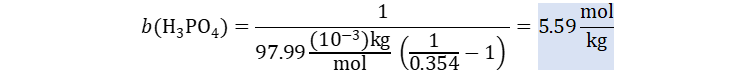

No hay comentarios:
Publicar un comentario